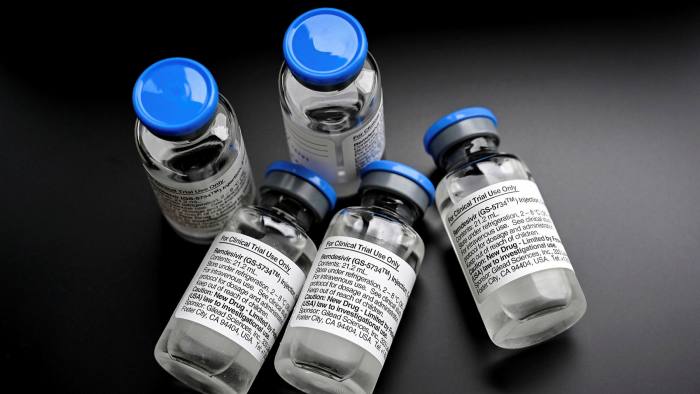
Anche se Remdesivir può ridurre il tasso di mortalità e la durata della malattia COVID-19, non è considerato del tutto efficace. Tuttavia, le autorità statunitensi hanno ora approvato il farmaco per l’uso contro la malattia.
 La Food and Drug Administration (FDA) statunitense ha approvato il farmaco Remdesivir per il trattamento di COVID-19, rilasciando una dichiarazione venerdì 23 ottobre. Il farmaco era stato precedentemente approvato negli Stati Uniti solo con un’approvazione d’emergenza (EUA). In Europa, il prodotto aveva anche ricevuto un EUA a luglio per il trattamento di alcuni pazienti affetti da COVID-19.
La Food and Drug Administration (FDA) statunitense ha approvato il farmaco Remdesivir per il trattamento di COVID-19, rilasciando una dichiarazione venerdì 23 ottobre. Il farmaco era stato precedentemente approvato negli Stati Uniti solo con un’approvazione d’emergenza (EUA). In Europa, il prodotto aveva anche ricevuto un EUA a luglio per il trattamento di alcuni pazienti affetti da COVID-19.
Remdesivir è stato messo a fuoco come potenziale cura subito dopo che le prime infezioni del nuovo coronavirus sono state segnalate in Cina. Remdesivir è stato originariamente sviluppato per trattare le infezioni da Ebola, ma ha anche mostrato efficacia contro la SARS e i coronavirus MERS nei test di laboratorio. Il nuovo SARS-CoV-2 è considerato una variante del patogeno della SARS del 2002.
Il farmaco è stato sviluppato dalla società farmaceutica statunitense Gilead Sciences come GS-5734. All’inizio della pandemia, non è stato approvato da nessun paese.
Da allora è stato utilizzato nel contesto dell’uso d’emergenza, così come nel contesto di studi scientifici in numerosi Paesi. Gilead Sciences ha dato al farmaco il marchio Veklury nell’autunno del 2020.
Dopo che un primo studio clinico negli Stati Uniti ha mostrato risultati positivi nel maggio 2020, la FDA ha concesso l’EUA. Da allora, Remdesivir ha potuto essere utilizzato negli ospedali per il trattamento di singoli pazienti con la malattia polmonare COVID-19 al di fuori degli studi clinici.
Il 15 ottobre 2020 l’Organizzazione Mondiale della Sanità (OMS) ha pubblicato uno studio prestampato non revisionato su MedRxiv che mostra che Remdesivir riduce di poco il tasso di mortalità dei pazienti affetti da COVID-19. Lo studio è il risultato del cosiddetto “Trial di SOLIDARIETÀ” in cui sono stati valutati i dati di 11.266 pazienti.
Gilead Sciences in una dichiarazione ha sostenuto che, facendo pubblicare lo studio come prestampa, “i dati di questo studio globale a marchio aperto non sono stati sottoposti alla rigorosa revisione necessaria per consentire una discussione scientifica costruttiva”.
Nella stessa dichiarazione, la società ha fatto riferimento a un altro studio con 1062 volontari, che è stato recentemente pubblicato sul New England Journal of Medicine (NEJM), che ha dimostrato che Remdesivir potrebbe ridurre il tempo medio di guarigione da 15 a 10 giorni.
Gilead Sciences ha presentato una domanda di approvazione regolare del farmaco alla FDA il 7 agosto 2020.
Come funziona Remdisivir?
L’effetto antivirale del Remdesivir deriva dalla sua funzione di cosiddetto analogo nucleotide. Il principio attivo inibisce la RNA polimerasi (RdRp) di virus come l’Ebola e il MERS perché la sua struttura è simile ai blocchi di costruzione dell’RNA. Durante la replicazione del virus, questi vengono erroneamente incorporati nei filamenti genetici delle nuove copie del virus. Nuovi virus veramente funzionali non possono essere creati in questo modo.
Anche se Remdesivir non si è dimostrato veramente efficace nella lotta contro l’Ebola, gli esperimenti di coltura cellulare e i primi esperimenti sui macachi hanno dimostrato che ha avuto un effetto promettente contro i coronavirus SARS e MERS-CoV, che sono strettamente correlati alla SARS-CoV-2.
I primi studi clinici con Remdesivir condotti negli Stati Uniti e in Cina avevano lo scopo di dimostrare se il farmaco aiutasse anche contro il COVID-19.
La Casa Bianca celebra gli effetti positivi
I primi risultati positivi di un primo studio clinico randomizzato negli Stati Uniti sono stati annunciati il 29 aprile 2020 direttamente dalla Casa Bianca a Washington DC. Parlando di Remdesivir in una conferenza stampa con il presidente degli Stati Uniti Donald Trump alla Casa Bianca, il direttore del National Institute for Allergy and Infectious Diseases (NIAID), Anthony Fauci, ha poi dichiarato: “Questo sarà lo standard di cura”.
Un totale di 1.063 pazienti con diversi gradi di gravità della malattia avevano partecipato allo studio finanziato dalla NIAID, il ‘Adaptive COVID-19 Treatment Trial’, e sono stati trattati con Remdesivir o un placebo per 10 giorni.
In uno studio randomizzato in doppio cieco, né i medici curanti né i pazienti sanno chi viene iniettato quotidianamente con il principio attivo e chi riceve un placebo. Questo per evitare che qualsiasi aspettativa del farmaco possa distorcere i risultati effettivi.
I risultati sono stati simili, anche se non così chiari come quelli del nuovo studio del NEJM. Secondo il NIAID, i risultati preliminari suggerivano che i pazienti di COVID-19 che ricevevano Remdesivir avevano, in media, un tempo di recupero più veloce del 31% rispetto ai pazienti cui era stato somministrato il placebo. I pazienti che hanno ricevuto il Remdesivir hanno avuto un tempo di recupero medio di 11 giorni e i pazienti che hanno ricevuto il placebo hanno avuto un tempo di recupero medio di 15 giorni.
Il tasso di mortalità nel gruppo trattato con Remdesivir è stato dell’8% rispetto all’11,6% del gruppo trattato con placebo. I responsabili delle sperimentazioni le hanno poi considerate sufficienti. I National Institutes of Health degli Stati Uniti hanno detto che i risultati erano abbastanza significativi.
Parallelamente ai rapporti di successo di Washington, ci sono stati ulteriori rapporti dalla Cina, dove Remdesivir è stato testato per la prima volta per la sua efficacia in studi clinici randomizzati a Wuhan su pazienti in unità di terapia intensiva che soffrono di gravi casi di COVID-19.
Alla fine, però, a Wuhan mancavano i pazienti necessari a causa di un forte calo delle nuove infezioni, e anche questo studio è stato terminato prematuramente, secondo un rapporto di The Lancet.
Cosa significano i risultati?
Entrambi i primi due studi, così come quelli più recenti, pubblicati e divulgati, sembrano indicare la stessa conclusione: Il principio attivo Remdesivir si è chiaramente dimostrato moderatamente efficace. Riduce il tasso di mortalità leggermente ma non in modo significativo e riduce la durata della malattia di alcuni giorni.
Anche se questo è incoraggiante, è ben lungi dall’essere il clamoroso successo che molti avevano sperato da quello che è stato descritto come il candidato farmaco più promettente fino ad oggi.
L’esperto tedesco di malattie infettive, Gerd Fätkenheuer, professore di medicina all’ospedale universitario di Colonia, si aspettava una rapida approvazione di Remdesivir dopo la pubblicazione dello studio NIAID a maggio. Stava conducendo uno studio clinico su Remdesivir con pazienti in Germania.
“Per i pazienti con una forma grave di questa malattia, questo studio dà la speranza che saranno in grado di guarire dall’infezione più rapidamente e in modo sicuro”, ha detto. “Il metro di valutazione per l’efficacia di potenziali altri farmaci sarà, in futuro, Remdesivir”.
“I risultati dello studio su larga scala SOLIDARIETÀ dell’OMS con 11.266 pazienti in tutto il mondo non sono del tutto inaspettati, ma non meno deludenti” ha detto Clemens Wendtner, primario di infettivologia e medicina tropicale dell’ospedale municipale di Monaco di Baviera.
“Nonostante la limitazione che ad oggi non sono disponibili dati dettagliati sul server di prestampa e che è ancora in corso un processo di peer review, si può affermare che lo studio non è riuscito a raggiungere il suo endpoint primario: Nessuno dei quattro farmaci testati – Remdesivir, idrossiclorochina, Lopinar/Ritonavir e IFN-ß1a – è in grado di ridurre la mortalità da COVID-19 nei pazienti sintomatici che necessitano di cure ospedaliere”, ha detto Wendtler a proposito dello studio più recente.
Questo articolo è stato originariamente pubblicato il 30 aprile 2020 – prima dell’approvazione di Remdesivir. Da allora è stato aggiornato per includere le ultime informazioni provenienti da recenti studi scientifici e l’ultima approvazione della FDA.
| Fonte: https://www.dw.com/ – Traduzione: Matteo Poggiali |
| Le foto presenti sul sito sono state in larga parte reperite su Internet e quindi valutate di pubblico dominio. Se i soggetti o gli autori avessero qualcosa in contrario alla pubblicazione, non avranno che da segnalarlo all’indirizzo e-mail admin@soccorritori.ch, lo Staff provvederà prontamente alla rimozione delle immagini utilizzate. |



