“Dottore mi vedi un tracciato?”
La testa di Alessandra fa capolino dalla porta della sala visita.
“Solo dopo il caffè” rispondo io, ironicamente, anche se non avrei tutti i torti dato che sono le 8 di una domenica
mattina di inizio estate.
“No dottorè, guardami il tracciato perché questa signora non mi piace per niente.”
”Cos’ha?”
”È una sincope!”
“Fammi un po’ vedere…”
L’ECG fa l’effetto di 10 caffe tutti insieme: “Falla entrare in sala!”.
La paziente si chiama Franca, ha 78 anni e al momento della visita si presenta lucida.
“Cosa le è successo signora?”
”Non saprei dottoressa, stavo preparando il caffè e mi sono ritrovata a terra, sono svenuta dicono, ma io non mi sono accorta di nulla”.
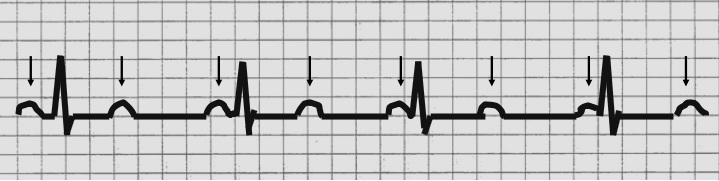
Sulle tracce dell’ECG
Franca ha una storia di episodi sporadici di fibrillazione atriale in trattamento con digitale, è ipertesa in terapia con beta bloccanti e ha una lieve insufficienza renale. La pressione è 95\50, l’obiettività clinica non mostra alterazioni di rilievo. La paziente viene monitorata, le vengono eseguiti dei prelievi ematici e posizionate le placche del pacing e soprattutto tranquillizzata.
Allerto il cardiologo per l’impianto del PM e poi vado da Alessandra “Vieni che ti offro il caffè!”.
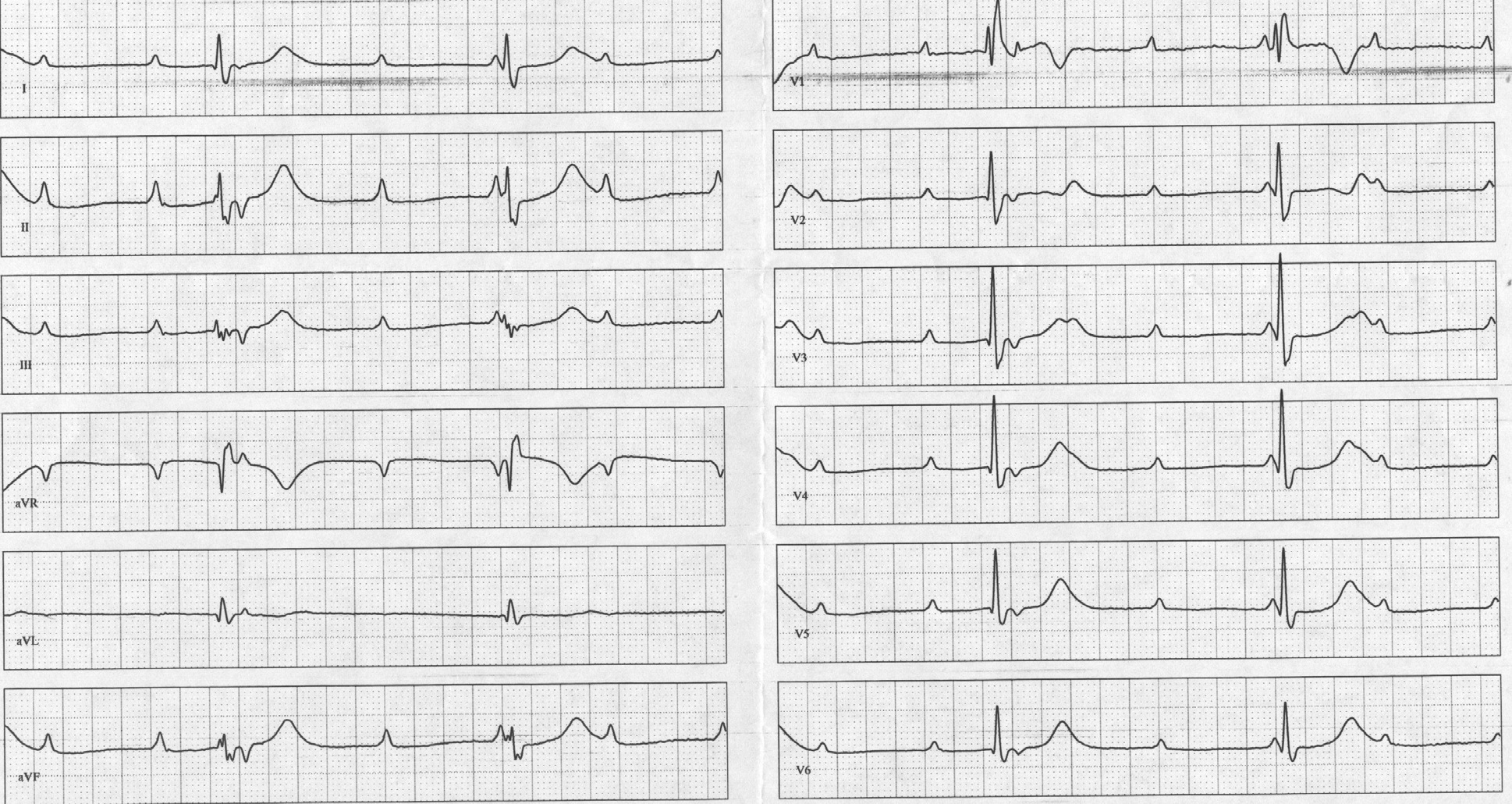
Interpretazione ECG: BAV di 3° grado (frequenza atriale 75 min, frequenza ventricolare circa 30 min) con BBds.
Questo caso clinico ci dà la possibilità di rivedere le aritmie ipocinetiche nelle quali più frequentemente un medico d’urgenza può imbattersi.
Si parla di BLOCCHI ATRIO VENTRICOLARI (BAV) quando la trasmissione verso i ventricoli dell’impulso cardiaco ad origine atriale viene rallentata, parzialmente bloccata o bloccata completamente. In base al rapporto tra onda P e complesso QRS vengono distinti tre tipi di BAV.
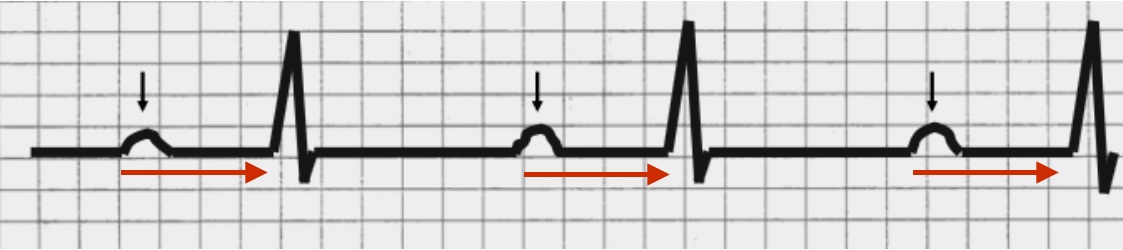
BAV I grado
È caratterizzato da un intervallo P-R prolungato oltre gli 0,20 sec. Ogni onda P è seguita da un complesso ventricolare, il che significa che ogni impulso a partenza dal nodo del seno arriva ai ventricoli. Normalmente benigno, non determina di solito alcuna complicazione, tuttavia il Framingham Heart Study ha rilevato un’associazione tra PR lungo e rischio di sviluppare fibrillazione atriale e necessità di avere bisogno in futuro di un pacemaker, con un piccolo incremento della mortalità proporzionale alla lunghezza dell’intervallo PR.
Quando è associato ad un blocco di branca destra ed emiblocco anteriore sinistro è espressione di un disturbo complesso della conduzione cardiaca che coinvolge sia la branca ds del fascio di His che i due fascicoli della branca sin (blocco trifascicolare) che facilmente evolve in situazioni che richiedeno la stimolazione cardiaca mediante pace maker.
BAV II
A differenza del BAV di I grado alcuni impulsi atriali non vengono condotti ai ventricoli. Sono correlati a patologia degenerativa del sistema di conduzione cardiaco e dovuti a diverse cause, tra queste le principali sono: cause iatrogene (beta-bloccanti, calci-antagonisti, digitale, antiaritmici, litio), cardiopatia ischemica, squilibri idroelettrolitici e metabolici, malattie infiammatorie (es. miocardite), ma anche malattie più rare di origine ereditaria come le distrofie muscolari.
Vengono distinti due tipi:
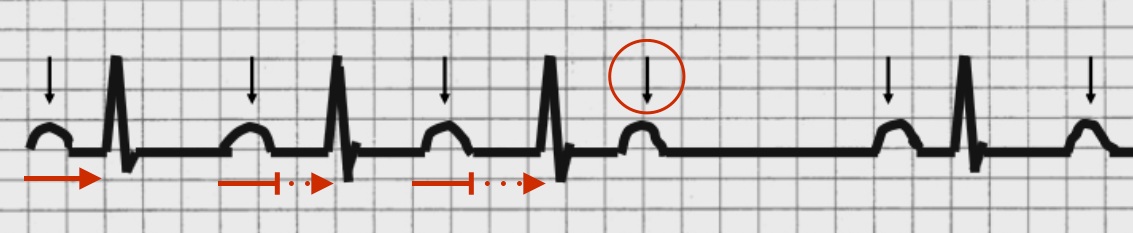
BAV II GRADO MOBITZ I
vi è un progressivo aumento dell’intervallo PR fino alla comparsa di un’onda P bloccata non seguita da un complesso QRS, il battito successivo ha un PR normale che successivamente ritorna ad allungarsi. Il complesso QRS è generalmente stretto.
È in genere migliorato dalla somministrazione di atropina e peggiorato dal massaggio del seno carotideo.
BAV II GRADO MOBITZ II
È caratterizzato dalla comparsa di un’onda P bloccata dopo un numero costante di battiti con intervallo PR normale.
Si possono avere BAV di II grado tipo Mobitz II con rapporto P:R di 2:1, 3:1, 3:2, 4:3. Il complesso QRS è slargato in circa l’80% dei casi.
È caratterizzato da:
• improvvisa mancata conduzione AV
• il PR che segue la pausa è identico a quello che precede il blocco
• la pausa che contiene la P bloccata è il doppio degli altri intervallo RR
In caso di blocco intra o sottohissiano l’atropina può peggiorare la conduzione È considerato più grave per la possibilità di progressione a blocco atrio-ventricolare avanzato.
BAV III Grado
Si verifica quando gli impulsi articoli non raggiungono in alcun modo i ventricoli. È caratterizzato dalla totale assenza di rapporto delle onde P con i complessi QRS che possono avere morfologia diversa a secondo dell’origine (ritmi di scappamento originati dalla giunzione atrioventricolari o ventricolari). Le onde P possono precedere, essere inscritte nel QRS o seguirlo. Il BAV di III riconosce diverse cause. Una percentuale variabile dal 5 al 15% degli infarti miocardici acuti può complicarsi con un BAV di III grado.
Nell’IMA inferiore il blocco completo è di solito preceduto da BAV di I grado o II grado, la sede del blocco è a livello del nodo AV ed è in genere transitorio.
Nell’IMA anteriore il blocco completo si verifica a seguito di danno esteso del ventricolo di sinistra, ed anche in questo caso viene in genere preceduto da BAV di II grado o blocchi bifascicolari. La tossicità da digitale è una delle cause più frequenti di BAV di III grado reversibile. L’iperpotassiemia severe può provocare un BAV di III grado, anche se in genere il decesso si verifica prima a causa di tachiaritmie ventricolari. I processi infiammatori del cuore (miocarditi ed endocarditi) possono essere causa di impedimento della conduzione cardiaca a causa dell’edema dei testi personali atrioventricolari. Altre cause più rare da tenere in considerazione sono le miocardiopatie infiltrati (amiloidosi e sarcoidosi), la contusione miocardica, la febbre reumatica, la valvulopatia aortica severa, malattie degenerative del sistema di conduzione (malattia di Lev-Lenegre), la Borreliosi di Lyme.
Arresto sinusale
Il nodo seno-atriale smette di mandare impulsi agli atri determinando un periodo di asistolia . Il successivo ciclo cardiaco inizia con un normale impulso dal nodo seno-atriale o con un impulso dal nodo AV (può essere presente retroconduzione atriale) o dalle vie di conduzione ventricolari. Se la pausa è prolungata può comparire un battito di scappamento. Può essere presente in soggetti con cuore normale. Si può verificare in presenza di aumentato tono vagale, miocardite, infarto miocardico e tossicità digitalica.
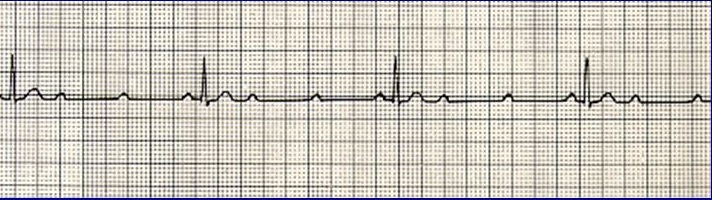
Bradicardia sinusale
È caratterizzata dalla riduzione della frequenza cardiaca al di sotto dei 50 battiti/minuto per l’adulto. Gli impulsi originano tutti dal nodo del seno con bassa frequenza. Gli assi elettrici, la durata del QRS, la morfologia dell’onda P, il PQ e QT sono normali. È data in genere da ipertono vagale, può essere dovuta a numerose patologie cardiovascolari e non cardiovascolari (da non dimenticare le cause iatrogene) e non sempre ha significato patologico.
Blocchi seno atriali
Vi è un rallentamento o un blocco della conduzione degli impulsi simulassi all’atrio. Se ne distinguono tre gradi.
Nel BSA di I grado la conduzione degli impulsi all’atro è solo ritardata e non è possibile far diagnosi all’ECG di superficie.
Il blocco senatoriale di II grado è a sua volta suddiviso in:
Nel BSA di II grado tipo I (Mobitz I) in cui vi è un progressivo accorciamento degli intervalli PP fino a che si verifica una pausa sinusale inferiore al doppio del ciclo di base.
È caratterizzato da:
• morfologia ed asse dell’onda P compatibile con origine dal nodo del seno
• accorciamento del PP che termina con una pausa
• PR costante
• pausa PP minore del doppio dell’intervallo PP normale
Nel BSA di II grado tipo II (Mobitz II) vi sono pause sinusali multiple rispetto agli intervalli PP. È caratterizzato da intervallo PP costante seguito da pausa multipla dell’intervallo PP normale
BSA III grado
Mancata conduzione senoatriale, in pratica non può essere distino dall’arresto sinusale completo. Solo l’emergenza di un battito da scappamento sopraventricolare o ventricolare evita l’asistolia.
Possono essere presenti nei soggetti sani con tono vagale aumentato, ma anche essere dovuti a cardiopatie sottostanti e verificarsi in caso di infarto miocardico inferiore e tossicità digitalica.
La gestione clinica della bradicardia si basa innanzi tutto sulla differenziazione tra bradicardia sintomatica ed asintomatica. Nella valutazione iniziale infatti bisogna valutare se la bassa frequenza cardiaca sia emodinamicamente significativa e sia quindi la causa alla base del quadro clinico di presentazione. Si rende necessario un trattamento della bradicardia solo quando questa sia la causa che origina i segni od i sintomi clinici.
I segni clinici che possono essere causati dalla bradicardia includono:
• stato mentale alterato acutamente;
• dolore toracico ischemico;
• scompenso cardiaco congestizio;
• ipotensione;
• segni di shock (che persistono nonostante una adeguata via aerea sia garantita e respiro appropriato).
Il primo passo nella gestione della bradicardia è dato dalla identificazione di possibili cause scatenanti e dal loro trattamento. Innanzi tutto deve essere quindi garantita la pervietà delle vie aeree ed una adeguata ventilazione.
Se un’adeguata ossigenazione non permette un miglioramento della frequenza od una regressione dei sintomi, è indicato l’inizio di una terapia farmacologica mirata.
Se la bradicardia genera uno o più dei segni e sintomi clinici, il trattamento farmacologico di prima linea è dato dalla somministrazione di atropina (classe IIa, LOE B). il nodo seno-atriale ed atrioventricolare sono innervati dal nervo vago, la cui azione di rallentamento del ritmo cardiaco e della conduzione è mediata dal rilascio di acetilcolina. L’atropina agisce bloccando l’effetto della acetilcolina rilasciata dal nervo vago, per cui le aree di miocardio non innervate dal nervo vago possono perciò non essere responsive alla somministrazione della atropina.
L’atropina è la terapia di prima linea per la bradicardia acuta sintomatica e nei blocchi AV di secondo grado tipo I sec. Wenckebach (in cui l’attività vagale è un fattore scatenante) in cui la atropina può essere in grado di diminuire il grado del blocco. Non bisogna fare affidamento nella atropina nei blocchi AV di secondo grado tipo 2 e nei blocchi di terzo grado con QRS largo, quando la sede del blocco è verosimilmente localizzata nel tessuto non nodale (come nella branca di His o più distalmente nel tessuto di conduzione). In questi casi verosimilmente non vi è risposta alla atropina e la terapia di preferenza è il posizionamento di un pacing transcutaneo o la somministrazione di agenti β-adrenergici.
In assenza di cause reversibili di bradicardia, l’atropina rimane la terapia di prima linea per la bradicardia acuta sintomatica, e deve essere considerata una misura temporanea quando si attende il posizionamento di un pacemaker transcutaneo o transvenoso. A livello di dosaggi, è stato dimostrato che la somministrazione di atropina 0,5 mg ev in bolo, ripetuta ogni 3-5 minuti fino ad un totale di 1,5 mg è efficace nell’aumentare la frequenza cardiaca e nel far regredire i sintomi clinici. Le linee guida AHA ACLS 2010 indicano come dosaggio massimale 3 mg (ottenuto con somministrazione di boli ripetuti di 0,5 mg). Deve essere ricordato che dosaggi inferiori agli 0,5 mg di atropina possono generare un rallentamento paradosso della frequenza cardiaca, e che perciò il dosaggio minimo indicato è di 0,5 mg.
L’atropina deve essere usata con cautela in presenza di ischemia coronarica acuta o in corso di infarto del miocardio poiché l’effetto tachicardizzante può peggiorare l’ischemia o aumentare l’area infartuata.
In caso di mancata risposta alla somministrazione di atropina in corso di bradicardia sintomatica, deve essere iniziato il pacing transcutaneo. Questa procedura non richiede particolari competenze invasive, e può essere eseguita dalla maggior parte del personale sanitario dopo un breve addestramento.
Il pacing transcutaneo si ottiene mediante la stimolazione elettrica del cuore con la somministrazione di un impulso elettrico con due elettrodi applicati sul torace, solitamente in sede toracica anteriore e posteriore. La frequenza cardiaca target deve essere identificata come la minore sufficiente a garantire una regressione dei sintomi (solitamente attorno ai 60-70 battiti al minuto). Poiché la procedura può essere dolorosa, qualora vi sia scarsa tolleranza del paziente deve essere considerata la somministrazione di farmaci analgesici o sedativi, con particolare attenzione però al potenziale effetto cardiologico dei farmaci utilizzati. Proprio alla luce della scarsa tolleranza alla procedura da parte dei pazienti, questa deve comunque sempre essere considerata una terapia ponte in attesa del posizionamento di un
pacing transvenoso.
Da rimarcare la controindicazione al pacing nel Pz ipotermico per l’alto rischio di indurre FV e per la difficoltà di trattamento di tale aritmia nell’ipotermia.
I più recenti defibrillatori in commercio possono essere utilizzati per il pacing transtoracico, ed hanno solitamente delle funzioni di base comuni a tutti:
• modalità di lavoro: a frequenza prefissata oppure a richiesta quando la frequenza cardiaca del paziente scende al di sotto di una soglia stabilita;
• frequenza cardiaca: con possibilità di scegliere una frequenza solitamente tra 30 e 180 impulsi al minuto;
• energia erogata: con possibilità di scegliere una potenza tra 0 e 200 mAmpere;
• durata dell’impulso elettrico: variabile tra 20 e 40 msecondi (solitamente setting modificabile solo dal produttore su richiesta del cliente);
• pulizia degli artefatti sul monitor. Questa funzione consente di eliminare dal monitor gli ampi spike indotti dal pacemaker in modo da non coprire la attività elettrica cardiaca sottostante. Questa funzione riveste una importanza cruciale, in quanto l’attività elettrica cardiaca deve essere sempre monitorizzata attentamente in corso di pacing, per il rischio di induzione di aritmie anche maligne a causa degli impusi elettrici erogati.
Dopo il posizionamento del pacing, devono essere valutate attentamente la presenza di cattura elettrica e la generazione di una efficace funzione meccanica cardiaca: infatti il pacing può fallire sia nel generare un impulso elettrico cardiaco (assenza di cattura elettrica) sia nel generare una efficace contrattilità cardiaca (assenza di cattura meccanica); per tale motivo la perfusione periferica e la pressione sistolica devono essere monitorizzate costantemente.
Anche se non è considerata la terapia di prima linea per la bradicardia sintomatica, la somministrazione di farmaci β-adrenergici è un’alternativa farmacologica quando non vi è risposta alla atropina o la risposta è inadeguata, od ancora può essere considerata come terapia provvisoria in attesa del posizionamento di un pacemaker.
In alcune circostanze particolari, come nel caso di bradicardia a intossicazione da β-bloccanti o di calcio-antagonisti, la somministrazione di β-adrenergici è particolarmente indicata come antidoto. ma questi principi hanno anche effetti indesiderati come ipotensione (la dobutamina) e la insorgenza di aritmie ventricolari (la adrenalina).
L’adrenalina è somministrata a dosaggi da 2 a 10 mcg al minuto in infusione continua, e deve essere titolata sulla base della frequenza cardiaca e della pressione arteriosa ottenute. La dopamina può essere utilizzata in pazienti con bradicardia sintomatica soprattutto se associata ad ipotensione (classe IIb, LOE B). Il dosaggio, di 2-10 mcg/kg al minuto in infusione continua IV, deve essere titolato sulla base della risposta clinica ottenuta. Bisogna sempre ricordare che la dopamina somministrata a basso dosaggio induce una vasodilatazione splancnica con conseguente ipotensione, e quindi se è somministrata a dosaggi ridotti deve essere sempre associata ad un adeguato riempimento volemico. Deve essere inoltre ricordato che l’isoproterenolo e la dobutamina hanno un effetto β1-agonista, con conseguente vasodilatazione associata all’incremento del ritmo cardiaco, più spiccata per l’isoproterenolo che per la dobutamina.
Se le terapie farmacologiche intraprese od il pacing transcutaneo devono essere continuate per mantenere una adeguata frequenza o perfusione, il paziente deve essere sottoposto al posizionamento in urgenza di un pacing transvenoso (classe IIa, LOE C). per il posizionamento del pacing transvenoso è necessaria una specifica competenza, che può anche essere acquisita mediante simulazione ad alta fedeltà.
| Fonte: Italian Journal of Emergency Medicine |
| Le foto presenti sul sito sono state in larga parte reperite su Internet e quindi valutate di pubblico dominio. Se i soggetti o gli autori avessero qualcosa in contrario alla pubblicazione, non avranno che da segnalarlo all’indirizzo e-mail admin@soccorritori.ch, lo Staff provvederà prontamente alla rimozione delle immagini utilizzate. |